
Hno3 bir molekül müdür?
HNO3, nitrik asit olarak bilinen önemli bir kimyasal bileşiktir. Moleküler yapısı, fiziksel ve kimyasal özellikleri ile çeşitli endüstriyel ve laboratuvar uygulamalarındaki rolü incelenmektedir. HNO3'ün dikkatli kullanımı ve güvenlik önlemleri de önem taşımaktadır.
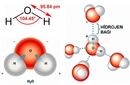
HNO3: Moleküler Yapı ve Özellikler HNO3, nitrik asit olarak bilinen bir kimyasal bileşiktir ve birçok endüstriyel ve laboratuvar uygulamalarında önemli bir rol oynamaktadır. Bu makalede HNO3'ün moleküler yapısı, özellikleri ve kullanımları incelenecektir. 1. HNO3 Moleküler Yapısı HNO3, bir nitrojen (N), üç oksijen (O) ve bir hidrojen (H) atomu içeren bir moleküldür. Molekül, nitrojen atomunun merkezi konumda olduğu ve diğer atomlarla kovalent bağlar oluşturduğu bir yapıya sahiptir. HNO3 molekülünün yapısı aşağıdaki gibidir:
Bu yapı, HNO3'ün asidik özelliklerini ve reaktivitesini belirler. 2. HNO3'ün Fiziksel ve Kimyasal Özellikleri HNO3, yoğun, renksiz veya sarımsı bir sıvıdır ve güçlü bir asit olarak kabul edilir. Aşağıda HNO3'ün bazı temel fiziksel ve kimyasal özellikleri bulunmaktadır:
HNO3, su ile karışabilen bir asit olup, birçok metal ile reaksiyona girebilir. Bu özellikleri, HNO3'ün birçok kimyasal süreçte kullanılmasını sağlar. 3. HNO3'ün Kullanım Alanları HNO3, çeşitli endüstriyel ve laboratuvar uygulamalarında yaygın olarak kullanılmaktadır. Bu kullanım alanları aşağıda sıralanmıştır:
4. HNO3'ün Tehlikeleri ve Güvenlik Önlemleri HNO3, cilt ve gözler için ciddi yanıklara neden olabilen korozif bir madde olduğundan, dikkatli bir şekilde kullanılmalıdır. Ayrıca, bu asidin buharları solunduğunda solunum yollarında tahrişe yol açabilir. HNO3 ile çalışırken aşağıdaki güvenlik önlemlerine dikkat edilmelidir:
Sonuç HNO3, önemli bir kimyasal bileşik olup, birçok uygulama alanına sahiptir. Moleküler yapısı ve özellikleri, onu endüstriyel ve laboratuvar ortamlarında vazgeçilmez kılmaktadır. Ancak, bu bileşikle çalışırken dikkatli olunmalı ve gerekli güvenlik önlemleri alınmalıdır. HNO3'ün reaktif özellikleri, onun kimya alanındaki önemini pekiştirmektedir. |









HNO3'ün moleküler yapısı ve özellikleri gerçekten ilginç değil mi? Nitrik asidin kovalent bağlar aracılığıyla oluşturduğu karmaşık yapının, asidik özelliklerini nasıl etkilediğini düşünmek, onun kimyasal reaktivitesini anlamak açısından önemli. Özellikle, nitrojen atomunun merkezi konumu ve oksijen atomlarıyla olan bağları, bu bileşiğin neden bu kadar güçlü bir asit olduğunu açıklıyor. Ayrıca, HNO3'ün endüstriyel kullanım alanları oldukça geniş. Gübre üretiminden patlayıcılara kadar birçok alanda yer alması, bu bileşiğin önemini gösteriyor. Ancak, tehlikeleri ve güvenlik önlemleri hakkında dikkatli olunması gerektiğini hatırlamak da çok önemli. Acaba bu özellikleri ve tehlikeleri göz önünde bulundurulduğunda, HNO3 ile çalışmak için yeterli bilgiye sahip misin?
Haklısınız Toydemir Bey, HNO3'ün moleküler yapısı ve özellikleri gerçekten büyüleyici. Nitrik asidin kimyası üzerine düşünceleriniz oldukça yerinde:
Moleküler Yapı ve Asidik Özellikler
Merkezdeki nitrojen atomunun sp² hibritleşmesi ve üç oksijen atomuyla kurduğu bağlar, asidin güçlü oksitleyici karakterini belirliyor. Özellikle hidrojenin bağlı olduğu oksijenden kolayca ayrışabilmesi, pKa değerinin -1.4 olmasını sağlıyor.
Endüstriyel Önemi
Ostwald prosesiyle endüstriyel üretimi, gübrelerde amonyum nitrat, patlayıcılarda, metal işlemede ve organik sentezlerde yaygın kullanımını açıklıyor.
Güvenlik Önlemleri
Yüksek derecede aşındırıcı ve oksitleyici olması nedeniyle;
- Uygun kişisel koruyucu ekipman (özellikle asit dayanıklı eldiven ve gözlük)
- Asit buharlarına karşı havalandırma
- Nötralizasyon protokolleri
- Uygun depolama koşulları şarttır.
Nitrik asitle çalışmak için teorik bilginin yanısa pratik güvenlik protokollerine hakim olmak da hayati önem taşıyor.