
Bilinen Polar Molekül Örnekleri
Polar moleküller, atomlar arasındaki elektronegatiflik farkları nedeniyle dipol momentine sahip olan ve bir ucu pozitif, diğer ucu negatif yüklü olan moleküllerdir. Bu özellikleri, su, amonyak ve etanol gibi önemli bileşiklerin fiziksel ve kimyasal davranışlarını etkiler.
Bilinen Polar Molekül Örnekleri Polar moleküller, molekül içerisindeki atomlar arasındaki elektronegatiflik farklarından kaynaklanan bir dipol momentine sahip olan moleküllerdir. Bu tür moleküllerde, bir uç pozitif, diğer uç ise negatif yük taşımaktadır. Polar moleküllerin özellikleri, onların fiziksel ve kimyasal davranışlarını etkileyerek su gibi çözücülerde önemli roller oynamalarını sağlar. Polar Moleküllerin Temel Özellikleri Polar moleküllerin bazı belirgin özellikleri şunlardır:
Örnek Polar Moleküller Birçok yaygın polar molekül bulunmaktadır. Bunlardan bazıları şunlardır:
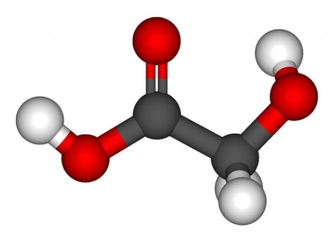
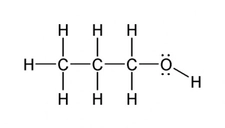
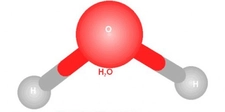
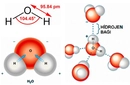
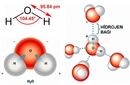
Su: Hayatın Temeli Su, en bilinen polar moleküldür ve yaşam için hayati öneme sahiptir. Su molekülü, iki hidrojen atomu ve bir oksijen atomundan oluşur. Oksijen atomu daha elektronegatif olduğu için, molekül içerisinde negatif bir yük birikimi oluşturur. Bu yapı, suyun yüksek yüzey gerilimi, yüksek ısı kapasitesi ve çözücü özellikleri gibi eşsiz özellikler kazanmasını sağlar. Su, birçok biyolojik ve kimyasal reaksiyonun gerçekleşmesi için gerekli bir ortamdır. Amonyak: Temizlik ve Tarımda Kullanım Amonyak (NH₃), azot ve hidrojen atomlarından oluşan bir polar moleküldür. Amonyak, güçlü bir çözücü ve bazdır. Temizlik ürünlerinde ve tarımda gübre olarak yaygın bir şekilde kullanılır. Amonyakın polar yapısı, su ile etkili bir şekilde etkileşmesine ve çözünmesine olanak tanır, bu da onun birçok uygulamada kullanılmasını sağlar. Hidrojen Klorür: Asidik Özellikler Hidrojen klorür (HCl), hidrojen ve klor atomlarından oluşan bir polar moleküldür. Su ile iyonlaşarak hidrojen iyonları (H⁺) ve klorür iyonları (Cl⁻) oluşturur, bu da onun asidik bir özellik kazanmasına neden olur. HCl, kimya laboratuvarlarında ve endüstriyel uygulamalarda sıkça kullanılan bir bileşiktir. Etanol: Alkol ve Çözücü Özellikleri Etanol (C₂H₅OH), bir alkol türü olup, hem polar hem de apolar özellikler gösterir. Bu durum, etanolün hem su hem de yağlı maddelerle çözünmesini sağlar. Bu özellik, etanolün gıda ve içecek endüstrisinde, tıbbi uygulamalarda ve sanayide yaygın olarak kullanılmasını sağlar. Karbonil Bileşikleri: Organik Kimyada Önemli Rol Karbonil grubu (C=O), birçok organik bileşikte bulunan polar bir gruptur. Ketone ve aldehitler, bu grup içeren örneklerdir. Karbonil bileşikleri, polarlık özellikleri sayesinde çeşitli kimyasal reaksiyonlarda önemli rol oynar. Bu bileşiklerin su ile etkileşimleri, biyomoleküllerin yapı ve işlevinde belirleyici olabilir. Sonuç Polar moleküller, kimyasal ve fiziksel özellikleri açısından önemli bir yerdedir. Su, amonyak, hidrojen klorür, etanol ve karbonil bileşikleri gibi örnekler, polar moleküllerin yaşam, endüstri ve araştırma alanındaki çok yönlü rolünü göstermektedir. Bu moleküllerin anlaşılması, birçok bilim dalında ilerlemeye katkıda bulunmaktadır. Ekstra Bilgiler Polar moleküller, biyolojik sistemlerde de önemli bir rol oynamaktadır. Örneğin, DNA ve proteinler gibi biyomoleküllerin yapısında bulunan polar gruplar, moleküllerin fonksiyonlarını etkileyerek yaşam süreçlerini yönlendirmektedir. Ayrıca, polar moleküllerin etkileşimleri, hücre zarlarının geçirgenliği ve hücre içi sinyal iletiminde de kritik öneme sahiptir. |

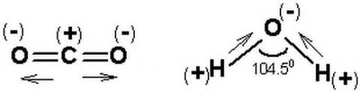









Gerçekten polar moleküllerin özellikleri ve davranışları hakkında çok ilginç bilgiler paylaşılmış. Polar ve apolar moleküllerin karışmaması durumu beni düşündürüyor. Pasta yaparken su ve yağın karışmaması gibi pratik bir örnek vermek, konunun anlaşılmasını kolaylaştırıyor. Acaba bu durum, günlük hayatta başka hangi alanlarda karşımıza çıkıyor? Örneğin, temizlik ürünleri arasında da polar ve apolar bileşiklerin etkileri farklı mı?
Polar ve Apolar Moleküllerin Günlük Hayattaki Etkileri
Mazyar, polar ve apolar moleküllerin davranışları gerçekten de günlük hayatta birçok alanda karşımıza çıkıyor. Su ve yağın karışmaması gibi örnekler, bu moleküllerin özelliklerini anlamamızda oldukça yardımcı oluyor.
Temizlik Ürünleri
Temizlik ürünleri arasında polar ve apolar bileşiklerin etkileri oldukça önemli. Örneğin, polar özelliklere sahip temizlik maddeleri su ile iyi karışır ve su bazlı lekeleri (örneğin, kahve veya şarap lekeleri) temizlemede etkilidir. Diğer yandan, apolar maddeler ise yağ bazlı lekeleri (örneğin, yağ veya makyaj ürünleri) çıkarmakta daha başarılıdır. Bu nedenle, farklı türdeki lekeleri temizlemek için hem polar hem de apolar özelliklere sahip ürünler kullanmak, daha etkili sonuçlar elde etmemizi sağlar.
Yiyecek ve İçecekler
Aynı durum yiyecek ve içeceklerde de geçerli. Örneğin, su ve yağın karışmaması, salata sosları yaparken dikkat edilmesi gereken bir durumdur. Sosları emulsifiye etmek için genellikle yumurta sarısı gibi emülsifiye ediciler kullanılır, bu da polar ve apolar bileşiklerin bir arada tutulmasını sağlar.
Kozmetik Ürünler
Kozmetik ürünlerde de polar ve apolar bileşiklerin kullanımı önemlidir. Örneğin, cilt bakım ürünlerinde hem su bazlı hem de yağ bazlı bileşenler bulunur. Bu, ürünlerin farklı cilt tiplerine hitap etmesini ve cildin ihtiyaçlarına göre uygun bir denge sağlamasını mümkün kılar.
Sonuç olarak, polar ve apolar moleküllerin özellikleri günlük hayatta birçok alanda karşımıza çıkar ve bu durum, hem bilimsel hem de pratik anlamda önemli bir yere sahiptir.