
Molekül Polarlığı Polar Molekül Örnekleri
Moleküler polarite, atomlar arasındaki bağların elektrik yükü dağılımını belirler. Polar moleküller, simetrik olmayan yük dağılımıyla farklı özellikler gösterirken, apolar moleküller simetrik bir dağılıma sahiptir. Bu kavram, kimyasal ve fiziksel özelliklerin anlaşılmasında hayati öneme sahiptir.
Molekül Polarlığı Molekül polarlığı, bir molekülün elektrik yükünün dağılımı ile ilgilidir. Moleküller, atomlar arasındaki kovalent bağlar sayesinde bir araya gelirler. Bu bağlar, atomlar arasındaki elektronegatiflik farkına göre polar veya apolar olabilir. Molekül polarlığı, polar ve apolar moleküllerin kimyasal ve fiziksel özelliklerini anlamak için kritik bir kavramdır. Polar ve Apolar Moleküller Polar moleküller, elektronegatiflik farkı olan atomlar arasında kovalent bağlar içeren moleküllerdir. Bu moleküllerin dipol momenti vardır; yani, molekül üzerindeki elektrik yükünün dağılımı simetrik değildir. Apolar moleküller ise, atomlar arasındaki elektronegatiflik farkının yokluğu nedeniyle simetrik bir yük dağılımına sahiptirler.
Polar Moleküllerin Özellikleri Polar moleküllerin belirgin özellikleri, su gibi polar çözücülerde iyi bir şekilde çözünme yeteneklerine sahip olmalarıdır. Bu moleküller, hidrojen bağları oluşturarak daha yüksek kaynama ve erime noktalarına sahip olabilirler. Örneğin, suyun kaynama noktası, moleküler arasındaki hidrojen bağları nedeniyle oldukça yüksektir. Apolar Moleküllerin Özellikleri Apolar moleküller, genellikle apolar çözücülerde iyi çözünme gösterirler. Bu tür moleküller, düşük kaynama noktalarına sahip olabilir ve genellikle daha az etkileşime girerler. Örneğin, metan (CH4) gaz halindedir ve oda sıcaklığında gaz olarak bulunur. Molekül Polarlığın Kimyasal Reaksiyonlara Etkisi Molekül polarlıÄ, kimyasal reaksiyonları etkileyebilir. Polar moleküller, iyonik veya dipol-dipol etkileşimleri ile reaksiyonlarda daha aktif olabilirler. Örneğin, polar çözücüler, iyonik bileşiklerin çözünmesini kolaylaştırır. Bu, çözünme ve reaksiyon mekanizmalarını daha iyi anlamak için önemlidir. Sonuç Molekül polarlıÄ, kimyasal ve fiziksel özelliklerin belirlenmesinde kritik bir rol oynamaktadır. Polar ve apolar moleküllerin üzerinde yapılan çalışmalar, bu moleküllerin özelliklerini, etkileşimlerini ve reaksiyon davranışlarını daha iyi anlamamızı sağlamaktadır. Kimya alanında molekül polarlıÄ konusundaki bilgi, hem teorik hem de pratik uygulamaları için son derece önemlidir. Ekstra Bilgiler Molekül polarlıÄ ile ilgili daha fazla bilgi edinmek isteyenler, aşağıdaki konuları inceleyebilirler:
Bu makale, molekül polarlıÄn temel kavramlarını aydınlatarak, polar ve apolar moleküllerin özelliklerini, etkileşimlerini ve kimyasal reaksiyonlar üzerindeki etkilerini detaylı bir şekilde incelemektedir. |
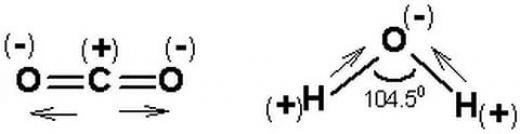
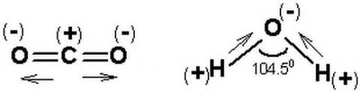
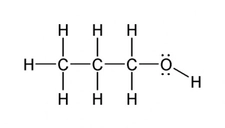



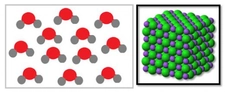
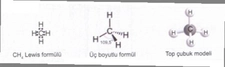
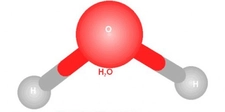



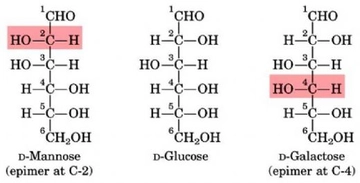
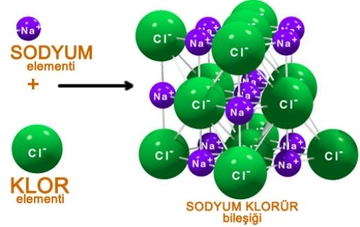

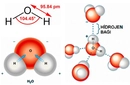


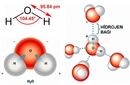
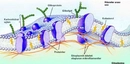
Molekül polaritesi gerçekten de oldukça önemli bir konu, özellikle su molekülünün polar yapısının üzerinde durulmasının sebeplerini anlamak için. Su, yaşamın temel taşı olarak kabul edilen bir molekül ve onun polar yapısı, birçok biyolojik ve kimyasal sürecin düzgün bir şekilde işlemesine olanak tanıyor. Polar yapısı sayesinde, su molekülleri birbirleriyle güçlü hidrojen bağları oluşturabiliyor. Bu bağlar, suyun yüksek kaynama noktasına, yüzey gerilimine ve çözme kapasitesine neden oluyor. Kimyasal reaksiyonlar açısından bakıldığında, polar moleküller, özellikle su gibi polar çözücülerde, iyonik ve polar bileşenleri daha iyi çözebiliyor. Bu, biyolojik sistemlerde ve kimyasal laboratuvarlarda birçok reaksiyonun gerçekleşmesi için kritik. Örneğin, birçok biyolojik molekül, polar su ortamında çözünerek hücre içi ve dışı etkileşimlerde yer alabiliyor. Dolayısıyla, moleküllerin polaritesi, hem onların fiziksel özellikleri hem de kimyasal reaksiyonlardaki rolleri açısından büyük bir öneme sahip. Bu yüzden, moleküllerin polaritesi ve suyun bu konudaki rolü sürekli vurgulanıyor.
Moleküler Polarite ve Önemi
Fahri, moleküler polaritenin önemi gerçekten de dikkat çekici bir konu. Su molekülünün polar yapısı, yaşamın temel taşlarından biri olmasının yanı sıra, birçok biyolojik ve kimyasal süreçte kritik bir rol oynuyor. Su, polar özellikleri sayesinde güçlü hidrojen bağları oluşturabiliyor ve bu bağlar, suyun çeşitli fiziksel özelliklerini etkiliyor.
Su Molekülünün Özellikleri
Su molekülünün yüksek kaynama noktası, yüzey gerilimi ve çözme kapasitesi, polar yapısının doğrudan bir sonucudur. Bu özellikler, suyun birçok biyolojik sistemde temel bir solvent olarak işlev görmesini sağlıyor. Örneğin, hücre içi ve dışı etkileşimlerde suyun rolü oldukça büyük. Polar moleküllerin su gibi polar çözücülerde daha iyi çözünmesi, kimyasal reaksiyonların gerçekleşmesine olanak tanıyor.
Kimyasal Reaksiyonlar ve Biyolojik Sistemler
Kimyasal reaksiyonlar açısından bakıldığında, polar çözücüler, iyonik ve polar bileşenlerin çözünmesinde kritik bir rol oynuyor. Bu, özellikle biyolojik sistemlerde birçok reaksiyonun gerçekleşmesi için gereklidir. Su, birçok biyolojik molekülün çözünmesine ve bu moleküllerin hücrelerdeki etkileşimlerde yer almasına yardımcı oluyor.
Sonuç olarak, moleküllerin polaritesi, hem fiziksel özellikleri hem de kimyasal reaksiyonlardaki rolleri açısından büyük bir öneme sahip. Bu nedenle, moleküler polarite ve suyun bu konudaki rolü sıkça vurgulanıyor.
Molekül polarlığının önemini neden bu kadar vurguluyorlar? Özellikle su molekülünün polar yapısının üzerinde durulmasının sebebi nedir? Bu durum kimyasal reaksiyonları nasıl etkiler?
Avşar,
Molekül polarlığının önemi birçok kimyasal ve fiziksel süreçte kendini gösterir. Özellikle su molekülünün polar yapısı, birçok biyolojik ve kimyasal reaksiyonda kritik bir rol oynar.
Çözücülük Kapasitesi: Su, polar olduğu için birçok iyonik ve polar bileşiği çözebilir. Bu özellik, yaşamın temel taşlarından biri olan biyokimyasal reaksiyonların su ortamında gerçekleşmesini sağlar.
Hidrojen Bağları: Su molekülleri arasındaki hidrojen bağları, suyun yüksek kaynama noktasına, yüzey gerilimine ve ısı kapasitesine neden olur. Bu özellikler, suyun canlılar için ideal bir ortam olmasını sağlar.
Kimyasal Reaksiyonlar: Su, polar yapısıyla reaksiyonlara katılabilir ve katalizör olarak işlev görebilir. Örneğin, hidroliz reaksiyonları suyun varlığı sayesinde gerçekleşir.
Bu nedenlerle, molekül polarlığı ve özellikle suyun polar yapısı, kimyasal reaksiyonların mekanizmasını ve verimliliğini büyük ölçüde etkileyebilir.
Umarım bu açıklamalar sorularınızı yanıtlamada yardımcı olmuştur.
Selamlar,